重庆大学李杨课题组JACS:芳炔1,2,3,5-四官能化研究
苯炔是一种重要的高活性有机中间体,可高效快捷地合成众多邻位二取代芳烃。然而,苯炔的形式三键特点决定了很难在苯炔环上炔键以外位点同时引入取代基。苯炔的这种内在结构限制在很大程度上阻碍了其在制备多取代苯中的应用。尽管“多苯炔”策略可在一定程度上打破这一限制,但其仍存在前体需要多步合成及反应中涉及区域选择性控制等问题。因此,利用简单苯炔实现苯环多取代的任务成为本领域亟待解决的问题之一。要实现这一目标,需要设计合适的串联过程,以便对苯炔环上其它位点进行选择性官能化。
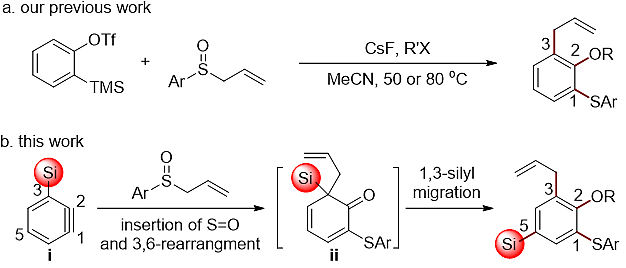
图1. 研究背景及课题内容
重庆大学李杨(点击查看介绍)课题组一直致力于苯炔化学新策略的探索,过去几年间通过多种策略实现了苯炔的多官能化转化(Acc.Chem.Res.,2020,53,508;J.Am.Chem. Soc.,2015,137,5670;J.Am.Chem.Soc.,2016,138,10814;J.Am.Chem.Soc.,2017,139,623;J.Am.Chem.Soc.,2018,140,3555;J.Am.Chem.Soc.,2018,140,13214;Angew.Chem.Int.Ed.,2019,58,18513;Chem.Soc.Rev.,2017,46,1707;Chem.Rev.,2021,asap,DOI:10.1021/acs.chemrev.0c01011)。其中,开发出首个利用简单苯炔制备1,2,3-三取代苯的串联转化(J. Am.Chem. Soc.,2016,138,10814)(图1a)。近日,他们进一步展示了利用3-硅基苯炔快速合成1,2,3,5-四取代芳烃的研究策略,该串联过程包含苯炔对亚砜S=O双键的插入、阴离子[3,6]-重排及苯环上的1,3-硅迁移过程(图1b)。值得指出的是,此反应中苯环上的1,3-硅迁移过程为首次发现。这一研究工作发表于《美国化学会会志》(J. Am. Chem.Soc.),蓝宇教授和李杨教授是论文共同通讯作者。
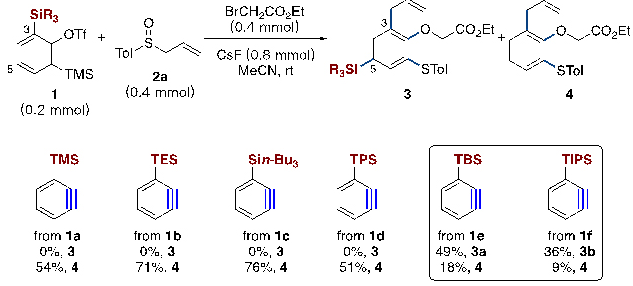
图2. 不同3-硅基苯炔与烯丙基亚砜的反应
在该研究工作中,他们首先对3-硅基取代的苯炔前体进行了筛选,发现当含硅基团是TMS、TES、n-Bu3Si及TPS时,得到的唯一产物是去硅基化产物4;而当使用二甲基叔丁基硅(TBS)或三异丙基硅(TIPS)时,得到1,2,3,5-四取代产物3(图2)。此一偶然发现,使简单苯炔反应与炔键远端位点(C5位)的官能化串联过程成为可能。
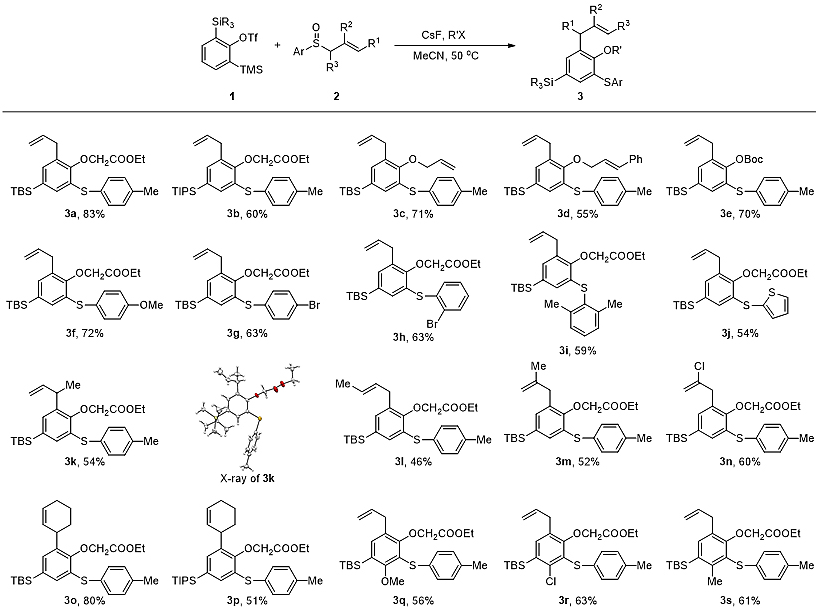
图3. 底物范围
经过条件优化及底物扩展,作者发现该3-硅基苯炔的1,2,3,5-四取代转化具有良好的官能团兼容性以及选择性,并且可用于合成最高五取代的芳香化合物3q-3s(图3)。进一步的研究表明,此芳环上的1,3-硅基迁移过程不仅限于上述反应体系。当2-TBS取代的苯酚6发生邻位溴化反应时,同样观测到硅基被溴取代并在苯环上发生1,3-迁移,得到相应产物7(图4)。
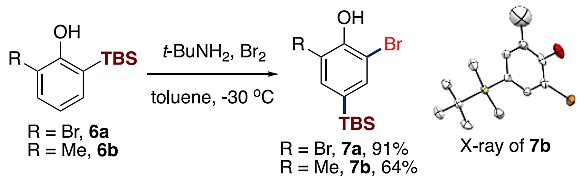
图4. 2-TBS苯酚在邻位溴化反应中的1,3-硅迁移
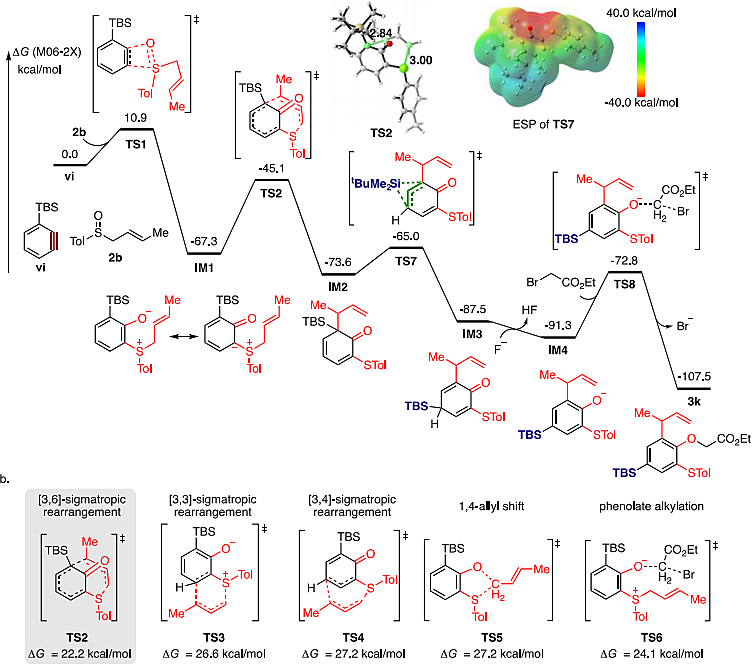
图5. DFT计算
随后,蓝宇教授和单春晖博士对可能的反应途径进行了计算。结果表明,该反应包含一个连续的苯炔对S=O双键的插入、10电子阴离子[3,6]-重排及苯环上的1,3-硅迁移过程(图5a)。针对重排反应步骤,比较了其它可能途径,例如[3,3]-重排,[3,4]-重排,1,4-烯丙基迁移以及酚氧烷基化反应,发现阴离子[3,6]-重排活化能最低(图5b)。同时发现,1,3-硅迁移步骤的活化能仅有8.6 kcal/mol,表明此转化可在较低温度下进行。这一发现与传统烯丙基硅的1,3-硅基热迁移明显不同,后者往往需要在较高温度下(>300 ℃)才可发生。对过渡态TS7的静电势能面(electrostatic potential surface)研究表明,此结构是一高度电荷分离结构,其中正电荷分布在硅基上,而负电荷集中于酚氧上,从而可大幅降低反应活化能。因此,此1,3-硅迁移可被视为是一个准协同过程。
小结
李杨教授与蓝宇教授合作,通过简单苯炔的串联过程,实现了苯环上的1,2,3,5-四官能化转化,突破了简单苯炔反应只能进行苯环邻位二取代的限制,扩展了苯炔化学在制备多取代芳香烃中的应用范围。石佳荣、李良贵及单春晖为本文的共同第一作者。此研究受到了国家自然科学基金委的项目资助((21901025,21971028,21772017,21822303)。
来源:X-MOL

